Aristocráticos gases (Miguel Carreras) –
Miradlos: a la derecha, los gases nobles-en rojo-, como
los domingos, como los días de descanso, porque rehúsan
combinarse y son ociosos y tranquilos.
(Del poema La tabla periódica, de David Jou en La escrituras del universo)
Dimitri I. Mendeleev , con su tabla, introdujo el necesario orden químico constatando que las propiedades de los elementos eran función periódica de las masas atómicas y la Química se hizo adulta como ciencia. Uno de los inconvenientes que presentaba la ordenación original era la no inclusión de los gases nobles (inertes o raros como se les llamaba en el pasado), prácticamente desconocidos en aquellos años. Posteriormente se enmendó el criterio ordenador y se les ubicó en el grupo 0, como cerovalentes, pese a las resistencias iniciales del ruso.
Según ha escrito Pascual Román, Mendeleev, al observar una gran diferencia de pesos atómicos entre un halógeno y el siguiente metal alcalino, en comparación con la existente entre cada par de elementos consecutivos, pudo admitir que eran posibles en principio elementos desconocidos situados entre ambas familias, pero en principio eran rebeldes a la clasificación y rompían la simetría de la tabla, con el problema añadido de la dificultad de determinación de pesos atómicos en elementos que no se combinaban. De hecho, al descubrirse el argón, Mendeleev llegó a decir que no era un elemento nuevo sino que se trataba de nitrógeno triatómico.
Una vez aceptados, William Ramsay y otros completaron este grupo de peculiares elementos de baja reactividad y que por tanto presentaban muy escasa tendencia a formar compuestos. Los gases nobles son estables, con un elevado potencial de ionización.
La configuración electrónica del Helio es 1s2 y la del resto de gases inertes, en el último nivel, es ns2 np6 , siendo n igual a 2,3,4,5 y 6, correspondiente al periodo de la tabla en el que se encuentra. Todos los demás elementos, al combinarse mediante distintos tipos de enlace, buscan alcanzar la estructura del gas noble más próximo en el sistema periódico.
La espectroscopia y el alumbramiento de los gases nobles.
Un físico no muy conocido, David Alter, estudiando el comportamiento de la luz con gases y metales, sugirió que cada elemento tenía su propio espectro y, poco después, en 1859, Robert W. Bunsen y Gustav R. Kirchoff presentaron su invento, el espectroscopio. La espectroscopia fue la técnica que facilitó el descubrimiento de un buen número de elementos, entre ellos los gases nobles.
Aunque en 1785 Henry Cavendish realizó un experimento que inducía a pensar que en el aire había algo más que oxígeno y nitrógeno, se tardaría más de un siglo hasta que Ramsay, haciendo pasar el nitrógeno obtenido del aire sobre magnesio al rojo, halló un gas residual que no se unía con ningún otro elemento. Al analizar su espectro de líneas rojas y verdes nunca observadas, junto a lord Rayleigh, anunciaba en 1894 el primer gas noble, el argón (inactivo en griego).
El espectroscopio permitió también descubrir el helio en el sol. Norman Lockyer comprobó en 1868 que una línea amarilla del espectro solar no pertenecía a ningún elemento conocido y le puso el nombre de helio y se creyó que solo aparecía en el sol. Ramsay y William Crookes ratificaron el hecho años más tarde.
Tras ser alumbrados helio y argón, había la convicción de la existencia de una familia de elementos inertes y en su búsqueda siguió empeñado Ramsay junto a su ayudante William Travers. Recurrieron al aire líquido, evaporándolo y eliminando con cobre y magnesio al rojo el nitrógeno y oxígeno, resultando un resto gaseoso con nueva línea espectral amarillo-verdosa. Y así, en 1898 fue presentado en sociedad el kriptón (oculto, escondido).
El hallazgo del kriptón no frenó las investigaciones en curso, pues esperaban algún elemento más ligero y el éxito acompañó unos meses después con la aparición del neón (nuevo) y el xenón (extraño).
La serie se completó cuando en 1900 Friedrich E.Dorn dedujo que en la desintegración del radio se producía, entre otros, un gas al que originalmente se denominó nitón y emanación y más tarde el actual de radón. Posteriormente se descubrieron dos isótopos del radón, el actinón y el torón.
En 1904 se concedió el Premio Nobel de Física a Rayleigh y el de Química a Ramsay, especialmente por las investigaciones citadas.
Obtención y propiedades .
 Primo Levi escribió en el primer capítulo de su libro El sistema periódico: “En el aire que respiramos existen los llamados gases inertes. (…) También se llaman gases nobles, aunque aquí se podría discutir si todos los nobles realmente son inertes y si todos los inertes son nobles”
Primo Levi escribió en el primer capítulo de su libro El sistema periódico: “En el aire que respiramos existen los llamados gases inertes. (…) También se llaman gases nobles, aunque aquí se podría discutir si todos los nobles realmente son inertes y si todos los inertes son nobles”
Los gases nobles se encuentran en la atmósfera, menos el radón, siendo el argón el que tiene más presencia (mayor que el dióxido de carbono) y el xenón el que menos. El helio también está en algunos hidrocarburos gaseosos naturales, procedente de elementos radiactivos de las rocas y parte de él se produce en las desintegraciones alfa en el sol (viento solar). Los isótopos del radón son todos radiactivos y. el de vida más larga se forma durante la descomposición del radio.
El radón se obtiene separando el gas que se forma a partir de soluciones de cloruro de radio. Todos los demás pueden obtenerse como productos del fraccionamiento del aire líquido. El helio se puede formar además mediante reacciones nucleares.
La química de los gases nobles se limita casi exclusivamente a las reacciones del xenón. Aunque Linus Pauling en 1933 predijo posibles compuestos de gases nobles, no fue hasta casi treinta años después cuando Neil Barlett y Howard Claassen obtuvieron por primera vez fluoruros y oxocompuestos de xenón:
F2 (g)+ Xe (g) → XeF2 (g).
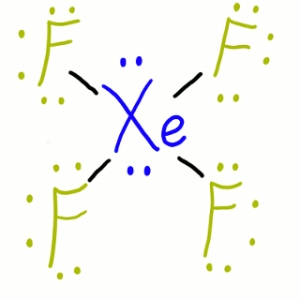
Se trabajó en vasija de níquel, a 400ºC y 1 atmósfera de presión. A 600ºc y 6 atm se producía tetrafluoruro de xenón y a 300ºC Y 60atm, el hexafluoruro. Éste último, con el agua, da lugar a un explosivo trióxido de xenón. El difluoruro se puede obtener exponiendo a la luz solar una mezcla de flúor y xenón. También, en condiciones muy drásticas, se han podido sintetizar fluoruros de kriptón y de radón. Se estima poco probable que helio, neón y argón sean capaces de reaccionar ni siquiera con el flúor.
 Antes de 1962 ya se habían conseguido unas agregaciones o complejos, los clatratos (compuestos jaula), en los que determinadas moléculas inorgánicas y orgánicas, encerraban en sus redes a todos los gases nobles, excepto helio y argón. Más recientemente se ha conseguido atrapar a los gases nobles en moléculas de fullereno.
Antes de 1962 ya se habían conseguido unas agregaciones o complejos, los clatratos (compuestos jaula), en los que determinadas moléculas inorgánicas y orgánicas, encerraban en sus redes a todos los gases nobles, excepto helio y argón. Más recientemente se ha conseguido atrapar a los gases nobles en moléculas de fullereno.
Los gases nobles, a diferencia de los otros elementos gaseosos, son monoatómicos.
El helio de la naturaleza es mayormente el isótopo de nº másico 4, con una mínima proporción de 3 He. Éste, licuado, es un líquido normal, pero el primero, es un fluído con sorprendentes y casi exclusivas propiedades. A 4,18k es el He I, con las propiedades de líquido normal. Enfriando más aparece el He II, que puede formar delgadas películas de solo cientos de átomos. A causa de su baja viscosidad, si se le coloca entre dos recipientes concéntricos, puede fluir de uno a otro y también hacia arriba (superfluídez). Ha sido considerado por algunos científicos durante algún tiempo como el cuarto estado de la materia
Aplicaciones
En general, encuentran aplicación en variadas fuentes de luz, convencionales y láseres.
El helio se utiliza, por ser poco inflamable y por su baja densidad- el gas más ligero tras el hidrógeno-, para rellenado de globos y como gas de elevación en naves ligeras. Es un referente en la criogenia destinada a imanes superconductores y en las investigaciones encaminadas a la aproximación a temperaturas en el límite del cero absoluto.
El neón se emplea en la fabricación de anuncios luminosos y tubos electrónicos y de televisión y, líquido, como refrigerante industrial.
El argón se aplica en la industria del acero para agitar el hierro fundido y ajustar la proporción de carbono, y en los neumáticos de los coches de lujo para proteger la goma del ataque del oxígeno y para que sean menos ruidosos. Como gas inerte en la soldadura de arco y en tubos fluorescentes, al igual que el xenón y el kriptón.
El radón, que se produce en la desintegración de torio y uranio naturales y en las plantas nucleares, es nocivo para la salud y se controla su presencia en los materiales de construcción. Es usado en radioterapia para combatir los tumores malignos.
Los fluoruros citados se emplean como oxidantes y para el almacenamiento y transporte de gases nobles.
Bibliografía:
-Gillespie- Humphreys- Baird- Robinson. Química. Editorial Reverté. 2002.
-D.F. Shriver, P.W.Atkins, C.H.Langford. Química Inorgánica. Editorial Reverté. 2001.
-Pascual Román. El profeta del orden químico: Mendeleev. Editorial Nivola. 2002.
-Isaac Asimov. Los gases nobles. Editorial Plaza &Janés.1982.
-Theodore Gray. Los elementos (Una exploración visual de todos los átomos que se conocen en el universo).Editorial Vox. 2011.
Asociación Ciencia Viva.










Un artículo muy didáctico sobre los gases nobles y sus aplicaciones, y muy interesante también!
Publicado por Carmen Fernández | febrero 7, 2013, 12:01 pm